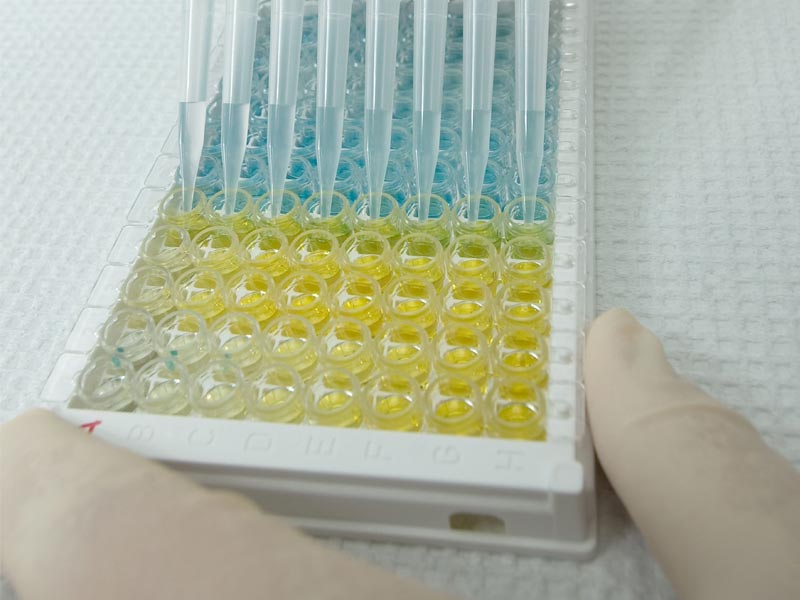
ELISA 加样操作要点
精准的仪器和准确的操作是保证ELISA结果准确关键,怎样的加样方式才是正确呢?ELISA实验中一般有5次加样,即加标本、加检测抗体、加酶结合物和加显色底物及终止液。小科将ELISA加样操作要点进行归纳,供参考。
- 实验室使用的微量加样器应注意保养并定期校正。ELISA比较敏感,每孔加入液体量误差会导致最后读数差别,因此避免仪器带来误差。
- 加样前,溶液充分混匀,垂直悬空加入液体,避免加在孔壁上,不可产生气泡。
- 加样时避免液体溅出,如有样本溅出,应用吸水纸轻轻拭干,并做相应记录。
- 如果加样枪漏气以至于加样的量不够,不能用枪吸出再加,做相应记录实验。
- 每次加样顺序一致,尤其底物、终止液顺序一致,保证每个孔显色时间相同。
ELISA 洗板操作要点
ELISA实验通过洗涤以清除残留在板孔中没能与固相抗原或抗体结合的物质,以及在反应过程中非特异性地吸附于固相载体干扰物质。因此,不严格的洗涤容易出现交叉污染或洗不干净背景高。 洗涤是ELISA实验操作最多一个步骤,如何洗板呢?
- 联科生物ELISA 洗液需要20倍稀释,配置时用新鲜无污染的蒸馏水或去离子水现配现用。洗液如果结晶应待其融解后配制。
- 垂直倒液,迅速、干脆,重复2-3次,不要手腕左右摇摆、旋转来倒液体。
- 倒液后将酶标板放在吸水纸拍干。用干净的滤纸,不要用卫生纸,因为细小粉尘或者碎屑容易吸附到孔底,导致洗板不干净,结果偏高或偏低,重复孔的数值也会相差很大。
- 每孔加300uL洗液,太多将溢出孔外污染相邻的孔。特别是每次洗板的前两遍,若高浓度孔流串到低浓度孔或空白孔,其造成的交叉污染将无法洗掉,背景增高。
- 加入洗液浸泡30s。洗板时间太短,洗涤效果不佳。延长洗板时间和增加洗板次数可以使背景更干净。
专题:ELISA 通关必备:
- 01. ELISA通关必备丨基础知识
- 02. ELISA通关必备丨试剂盒构成及检测原理
- 03. ELISA通关必备丨如何选择试剂盒
- 04. ELISA通关必备丨样本篇丨常见样本丨血清血浆
- 05. ELISA通关必备丨样本篇丨常见样本丨细胞
- 06. ELISA通关必备丨样本篇丨常见样本丨组织
- 07. ELISA通关必备丨样本篇丨不常见样本
- 08. ELISA通关必备丨操作篇丨溶解与稀释标准品
- 09. ELISA通关必备丨操作篇丨加样与洗板
- 10. ELISA通关必备丨操作篇丨常见问题及解决方案
- 11. ELISA通关必备丨结果篇丨白板与花板
- 12. ELISA通关必备丨数据篇丨数据分析与标曲拟合
- 13. ELISA通关必备丨数据篇丨标准曲线不佳