破骨细胞(osteoclast,亦称bone-resorbing cells)是骨组织成分的一种,行使骨吸收(bone resorption)的功能。成骨细胞(osteoblast,亦称bone-forming cells)是骨形成的主要功能细胞,负责骨基质的合成、分泌和矿化。
破骨与成骨过程的平衡是维持正常骨量的关键。破骨细胞与成骨细胞在功能上相对应。二者协同,在骨骼的发育和形成过程中发挥重要作用。破骨细胞的分化或激活主要受骨髓基质细胞或成骨细胞支持。骨疾病的发生与骨形成、骨吸收失衡有关,骨吸收大于骨形成导致骨量减少,导致骨质疏松症等,而骨吸收又与破骨细胞的数量和功能有关。
破骨细胞由多核巨细胞 (multi-nuclear giant cell, MNGC)组成,直径100μm,含有2~50个紧密堆积的核,主要分布在骨质表面、骨内血管通道周围,由多个单核细胞融合而成,胞浆嗜碱性,但随着细胞的老化,渐变为嗜酸性。
分离的破骨细胞具有如下特性:
1. 在体外迅速贴附于盖玻片或骨片;
2. 多核(一般为3~10个细胞核);
3. 伪足运动活跃,降钙素或降钙素基因相关肽可以抑制其伪足运动;
4. 酸性磷酸酶染色强阳性,酸性醋酸酯酶弱阳性,PAS中等阳性;
5. 细胞悬液与骨磨片共同培养,可以形成骨吸收陷窝;
来源
破骨细胞:造血祖细胞中的单核/巨噬系;
成骨细胞:间充质干细胞;
破骨细胞主要标志
高表达抗酒石酸酸性磷酸酶(TRAP, tartrate resistant acid phosphatase)和组织蛋白酶K (cathepsin K)。TRAP是破骨细胞特征性酶,其表达和分泌与破骨细胞功能密切相关,是破骨细胞重要的免疫组化识别标志。
破骨细胞的调控作用
骨吸收的力学行为与骨细胞中的破骨细胞紧密相关。破骨细胞是一种多核的大细胞,数量少于成骨细胞。在骨吸收的过程中,活跃的破骨细胞将会分泌酸性物质和酶,对矿化的骨基质进行分解吸收,使得该区域的骨量发生下降。骨吸收和骨生长同时存在,形成动态的平衡。当应力水平较低时,破骨细胞较成骨细胞活跃因而使得骨的总量发生下降,应力水平较高时则相反。

破骨细胞相关的细胞因子
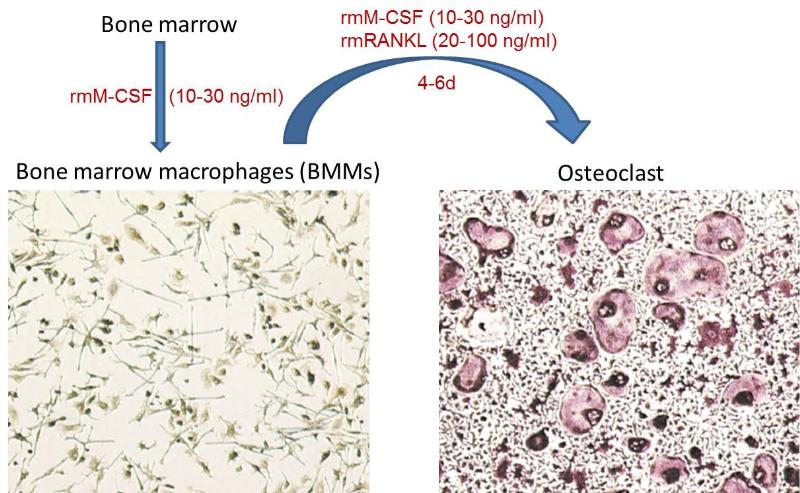
由前体细胞到破骨细胞需要 RANKL来掌控,而M-CSF能够促进分化过程中细胞的存活,骨髓来源的巨噬细胞 (BMM)向破骨细胞分化的过程中需要M-CSF和RANKL两种细胞因子的刺激,BMM表面受体RANK与c-fms可分别与成骨细胞等细胞产生的细胞因子RANKL和M-CSF结合,促使其向破骨细胞分化,另外成骨细胞还可以分泌OPG, 作为一种诱饵受体,竞争性与RANKL结合从来阻止RANKL和RANK结合来调节破骨细胞的生成。
许多趋化因子也被指出与破骨细胞的产生和功能有关,RANKL可以诱导CC类趋化因子,如CCL2, CCL3,CCL5和CCL9, 及 CXC趋化因子 (如CXCL10)等,由RANKL诱导产生的CCL2/MCP-1, 和CCL5/RANTES可以诱导TRAP阳性的多核细胞的产生。而CCL2可以逆转由GM-CSF所抑制的骨吸收过程。RANKL还可以上调CCL3及其受体CCR1的表达,二者可以促进破骨细胞的迁移。
CCL9/MIP-1γ 刺激破骨细胞的细胞质运动和细胞扩散。CXCL12/SDF-1可以促进破骨细胞化和骨吸收活性。RANKL诱导的CXCL10/IP-10的表达,在骨侵蚀性关节炎中,通过一种CD4+T细胞介导的机制发挥非常关键的作用。
核因子κ B受体活化因子配体
RANKL (Receptor Activator for Nuclear Factor-κ B Ligand),又名NF相关激活诱导细胞因子; osteo-protegerin ligand (OPGL), 骨保护素配体 (osteoclast differentiation factor, ODF),破骨细胞分化因子。RANKL是肿瘤坏死因子(tumor necrosis factor, TNF)超家族成员之一, 主要由成骨细胞系、T细胞和B细胞分泌。但也有一系列研究表明, 成骨细胞并不在破骨细胞的形成过程担当必要角色, 而骨细胞在破骨细胞的形成和活化过程中可能具有重要作用, 进而影响骨重建过程。最近发现, 在松质骨中骨细胞分泌的RANKL才是调节破骨细胞形成的主要来源,因此也有学者认为骨细胞对破骨细胞具有重要的调节作用。
巨噬细胞集落刺激因子
包括M-CSF (macrophage colony stimulating factor) 在内的细胞因子在破骨细胞成熟过程中具有不可或缺的调控作用。M-CSF最初由成骨细胞分泌产生, 可与髓系细胞上的相应受体结合并促进破骨细胞形成。M-CSF对于破骨细胞形成过程中基因谱的表达具有关键的调控作用。在信号传导方面, 它可通过ERK/Grb-2和Akt/PI3K信号通路调节破骨细胞前体细胞 (OCPs)的增殖、分化和存活。此外, M-CSF也可通过DAP12 (DNAX-activatingprotein 12, DAP12)和Syk (spleen tyrosine kinase, Syk)调节破骨细胞的骨吸收功能。
转化生长因子-β
TGF-β (transforming growth factor beta)是一种广泛分布于骨表面的细胞因子, 调节多种细胞生长和分化。TGF-β结合到两种不同类型的丝氨酸/苏氨酸激酶受体 (I型和II型受体)。II型受体与相应配体结合后, 通过下游Smad家族信号蛋白引起I型受体的磷酸化。TGF-β对破骨细胞的形成具有双向调节作用。一方面, TGF-β直接与骨髓巨噬细胞作用并促进破骨细胞形成。另一方面, TGF-β通过骨髓巨噬细胞周围的间充质细胞抑制破骨细胞形成。最新研究表明, TGF-β可以通过Smad3和TRAF6这两个信号分子调节RANKL引起的破骨细胞形成。
基质衍生因子
SDF-1 (stroma-derived factor-1)是破骨细胞前体迁移至骨吸收单位的过程中的关键细胞因子。在破骨细胞成熟过程中, 位于血液循环中OCPs细胞迁移至骨吸收单位并完成活化, 这是破骨细胞成熟的重要环节。SDF-1可以调节白细胞的迁移, 并且其局部浓度可以决定白细胞的定位, 由此调节OCPs的形成。例如, 在由TNF介导的炎症性关节炎中, TNF抑制间质细胞产生SDF-1导致来源于骨髓的OCPs进入血循环, 引起外周血循环过程中OCPs的数量增多。
骨保护素
OPG (osteoprotegerin)是骨吸收的主要负调节物。它由成骨细胞和其他类型细胞分泌。OPG的N-端具有半胱氨酸富集区域, C-端可以形成二聚体, OPG与RANKL结合进而阻止RANKL诱导的破骨细胞成熟。
PeproTech相关产品列表: