免疫治疗与化疗结合可以增加肿瘤的免疫原性,使肿瘤从“冷”到“热”,从而增强机体的内源性抗肿瘤反应,这已在多种恶性肿瘤的治疗中显示出很好的效果。利用某些化疗药物的免疫原性,如奥沙利铂、米托蒽醌、阿霉素、紫草素、硼替佐米、celastrol (Cel)、紫杉醇和吉西他滨,可以诱导免疫原性细胞死亡(ICD)。同时,免疫检查点封锁(ICB)治疗通过阻断免疫检查点使免疫抑制的肿瘤微环境正常化,从而增强抗免疫逃逸的有效性。化疗药物和ICB联合使用已被证明可以放大ICD的治疗效果。
Celastrol可以有效地诱导ICD,与7-乙基-10-羟基喜树碱(SN38,一种DNA拓扑异构酶I抑制剂)在诱导免疫原性细胞死亡和抗癌活性方面有很强的协同作用。然而,药物给药的不可控性和潜在脱靶毒性,有可能导致严重的全身副作用。目前,一些治疗性纳米药物已被用于靶向肿瘤的药物递送,以克服药物脱靶。
来自中国药科大学的研究团队在期刊《Chemical Engineering Journal》上发表了题为:Hypoxia-responsive immunostimulatory nanomedicines synergize with checkpoint blockade immunotherapy for potentiating cancer immunotherapy的研究论文,介绍了一种用于药物递送的缺氧敏感性纳米系统(命名为CS@TAP),并在CT26小鼠模型上证明了CS@TAP联合抗PD - L1单抗(αPD-L1)对肿瘤的治疗效果。
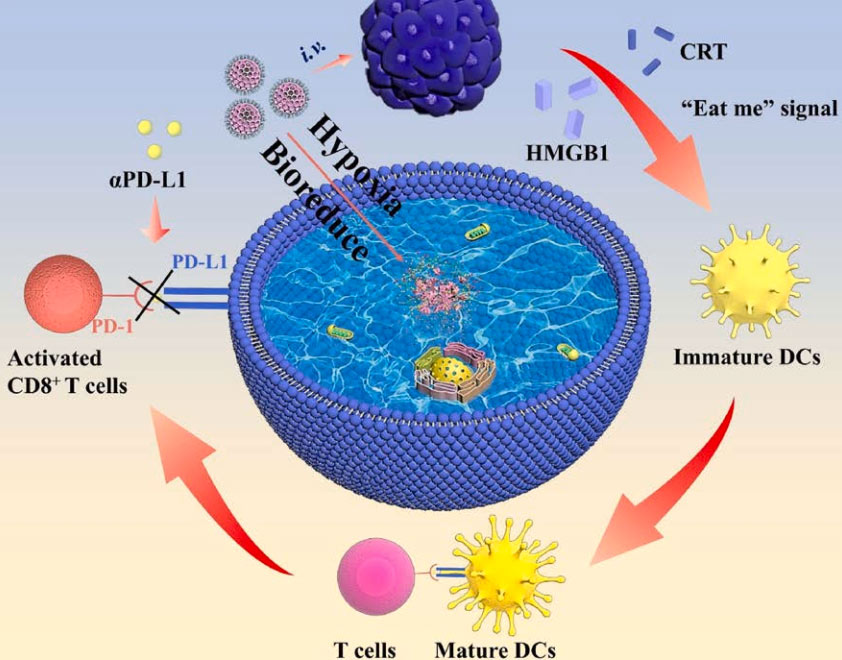
研究证明:CS@TAP是一个性能良好的纳米递送系统,可以有效克服药物的给药障碍。免疫原性细胞死亡的有效诱导,与肿瘤部位免疫细胞的有效招募密切相关,CS@TAP通过招募树突状细胞(DCs)至肿瘤部位,能够促进肿瘤相关抗原向T细胞的呈递,提高肿瘤部位细胞毒性T淋巴细胞(CTLs)的水平,以促进检查点封锁免疫治疗。αPD-L1可以阻断PD-1和PD-L1之间的相互作用,改善由于免疫逃避和T细胞耗竭而导致的肿瘤细胞免疫抑制。
这项研究提供了一种协同诱导免疫原性细胞死亡来增强细胞毒性T淋巴细胞浸润的策略,这种策略在抗肿瘤的免疫治疗方面具有巨大潜力。
MULTISCIENCES 产品支撑
流式抗体
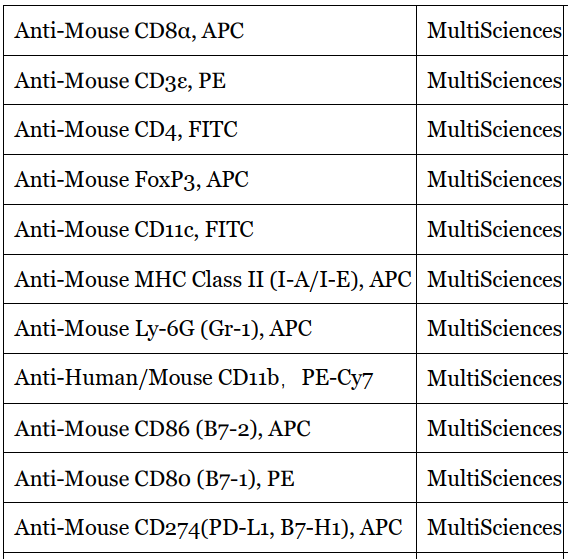
买流式抗体丨送同型对照
猛戳下图了解详情
更多相关产品和详细信息欢迎垂询和访问联科生物官网!